
Všetok obsah iLive je lekársky kontrolovaný alebo kontrolovaný, aby sa zabezpečila čo najväčšia presnosť faktov.
Máme prísne smernice týkajúce sa získavania zdrojov a len odkaz na seriózne mediálne stránky, akademické výskumné inštitúcie a vždy, keď je to možné, na lekársky partnerské štúdie. Všimnite si, že čísla v zátvorkách ([1], [2] atď.) Sú odkazmi na kliknutia na tieto štúdie.
Ak máte pocit, že niektorý z našich obsahov je nepresný, neaktuálny alebo inak sporný, vyberte ho a stlačte kláves Ctrl + Enter.
Deriváty zlúčenín talidomidu vedú k smrti rezistentných rakovinových buniek
Posledná kontrola: 02.07.2025
Štúdia, ktorú vykonala Goetheho univerzita vo Frankfurte, poukazuje na možnosť, že deriváty talidomidu by sa mohli potenciálne použiť na liečbu rakoviny. Talidomid sa v 50. rokoch 20. storočia predával ako tabletka na spanie. Neskôr sa stal známym tým, že spôsoboval závažné vrodené chyby v skorých štádiách tehotenstva.
Je tiež známe, že táto molekula označuje proteíny v bunke na deštrukciu. V rámci súčasnej štúdie vedci vytvorili deriváty talidomidu. Podarilo sa im preukázať, že tieto látky ovplyvňujú deštrukciu proteínov zodpovedných za prežitie rakovinových buniek.
Možno žiadna iná molekula nemala takú búrlivú minulosť ako talidomid. Bola hlavnou zložkou lieku schváleného v mnohých krajinách v 50. rokoch 20. storočia ako sedatívum a tabletka na spanie. Čoskoro sa však ukázalo, že tehotné ženy užívajúce talidomid často rodili deti so závažnými deformáciami.
V posledných desaťročiach však medicína opäť vkladá doň veľké nádeje. Štúdie okrem iného ukázali, že inhibuje rast ciev, a preto je potenciálne vhodný na odrezanie nádorov od ich živného média. Potom sa tiež ukázal ako veľmi účinný pri liečbe mnohopočetného myelómu, zhubných nádorov v kostnej dreni.
„Teraz vieme, že talidomid možno nazvať ‚molekulárnym lepidlom‘,“ vysvetľuje Dr. Xinglai Cheng z Inštitútu farmaceutickej chémie na Goetheho univerzite vo Frankfurte. „To znamená, že je schopný chytiť dva proteíny a spojiť ich.“
Toto je obzvlášť zaujímavé, pretože jeden z týchto proteínov je akýmsi „značkovacím strojom“: pripája k inému proteínu jednoznačné označenie „ODPAD“.
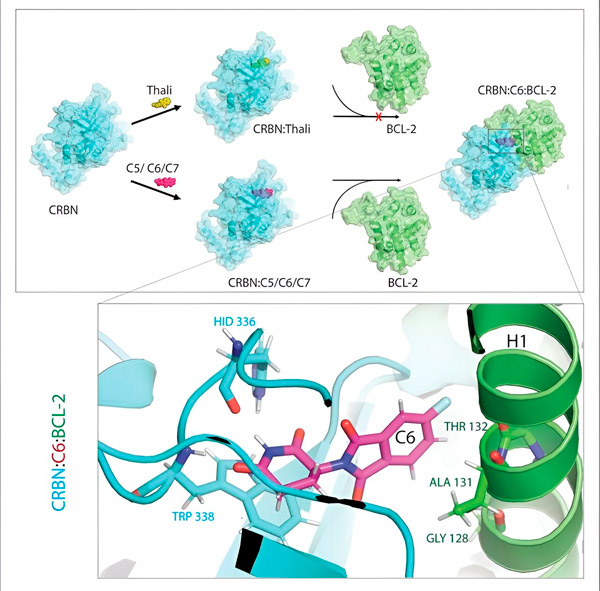
Deriváty talidomidu C5, C6 a C7 menia CRBN, „značkovací stroj“, tak, aby sa mohol viazať na BCL-2. Týmto spôsobom je molekula BCL-2 označená na degradáciu – čo je možná nová stratégia boja proti rakovine. Autor: Dr. Xinglai Cheng.
Systém bunkového odstraňovania odpadu rozpozná túto značku: Zachytí označenú molekulu proteínu a rozdrví ju. „Tento mechanizmus vysvetľuje rôzne účinky talidomidu,“ hovorí Cheng. „V závislosti od toho, ktorý proteín je označený, môže spôsobiť deformácie počas embryonálneho vývoja alebo zničiť malígne bunky.“
Tento mechanizmus otvára veľké možnosti pre medicínu, pretože rakovinové bunky sú na prežitie závislé od určitých proteínov. Ak by sa dali systematicky zacieliť a rozdrviť, možno by sa choroba dala vyliečiť. Problém je v tom, že molekulárne lepidlo je dosť zvláštne.
Jedným z jeho väzbových partnerov je vždy označovací stroj bunky alebo, vedecky povedané, E3 ligáza nazývaná CRBN. Len veľmi málo z mnohých tisícok proteínov v tele môže byť druhým partnerom – ktoré z nich závisia od lepidla.
„Vytvorili sme teda sériu derivátov talidomidu,“ hovorí Cheng. „Potom sme testovali, či majú adhezívne vlastnosti a ak áno, proti ktorým proteínom sú účinné.“ Vedci to dosiahli tak, že pridali svoje deriváty ku všetkým proteínom v kultivovanej bunkovej línii. Potom pozorovali, ktoré z týchto proteínov sa následne degradovali v prítomnosti CRBN.
„Počas tohto procesu sme identifikovali tri deriváty, ktoré by mohli označiť bunkový proteín BCL-2, ktorý je veľmi dôležitý pre degradáciu,“ vysvetľuje Cheng. „BCL-2 bráni bunkám v aktivácii ich programu sebazničenia, takže ak tam nie je, bunky odumierajú.“
Preto je BCL-2 už dlho predmetom výskumu rakoviny. Existuje dokonca liek na leukémiu s názvom venetoklax, ktorý znižuje účinnosť BCL-2, a tým spôsobuje samozničenie mutovaných buniek.
„V mnohých rakovinových bunkách je však samotný BCL-2 mutovaný. V dôsledku toho venetoklax už tento proteín neinhibuje,“ hovorí Cheng. „Dokázali sme, že aj naše deriváty signalizujú degradáciu tejto mutovanej formy. Naši partneri z Max Planck Institute for Biophysics navyše simulovali interakciu derivátov talidomidu s BCL-2 na počítači. Ukázalo sa, že deriváty sa viažu na úplne iné miesta ako venetoklax – výsledok, ktorý sme neskôr dokázali experimentálne potvrdiť.“
Výskumníci testovali svoje zlúčeniny aj na ovocných muškách s rakovinovými bunkami. Miera prežitia múch ošetrených týmto spôsobom bola výrazne vyššia. Cheng však varuje pred prílišnými nádejami, pretože tieto výsledky sú stále základným výskumom. „Hoci ukazujú, že modifikované molekuly talidomidu majú veľký terapeutický potenciál, zatiaľ nemôžeme povedať, či sa v praxi niekedy osvedčia.“
Výsledky štúdie boli publikované v časopise Cell Reports Physical Science.
